Profösör
Super Mod
- Katılım
- Ocak 11, 2022
- Mesajlar
- 3,752
- Etkileşim
- 29
- Puan
- 38
- Yaş
- 36
- Konum
- Rusya
- Web sitesi
- bilgilihocam.com
- F-D Coin
- 125
Tüm maddelerin kendine has belirli özellikleri vardır. Genellikle bu özellikleri ölçebilir ve maddenin boyutunu, ağırlığını veya bileşimini belirleyebiliriz. Örneğin, ahşabın çoğunlukla kahverengi olduğunu belirleyebilir, böylece renk özelliğini tespit edebiliriz. Bazı özellikler temel olarak kabul edilir ve bunlar çoğunlukla fiziksel ve kimyasal özelliklere ayrılır. Ayrıca maddenin genişlik ve yoğunluk özellikleri arasında ayrım yapılmaktadır.
Fiziksel Özellikler; Bir maddenin kimyasal bileşimini değiştirmeden ölçülebilen veya gözlemlenebilen özelliklerdir. Hacim ve renk gibi şeyler bu kategoriye girer.
Kimyasal Özellikler; Sadece bir maddenin kimyasal kimliğini değiştirdiğimizde ölçülebilir veya gözlemlenebilir.
Kapsamlı ve yoğun özellikler sadece fiziksel özelliklerdir, ancak iki özel gruba ayrılır. Hacim ve kütle gibi geniş özellikler, ölçtüğümüz madde miktarına bağlı olarak, renk ve yoğunluk gibi yoğun özellikler yoktur.
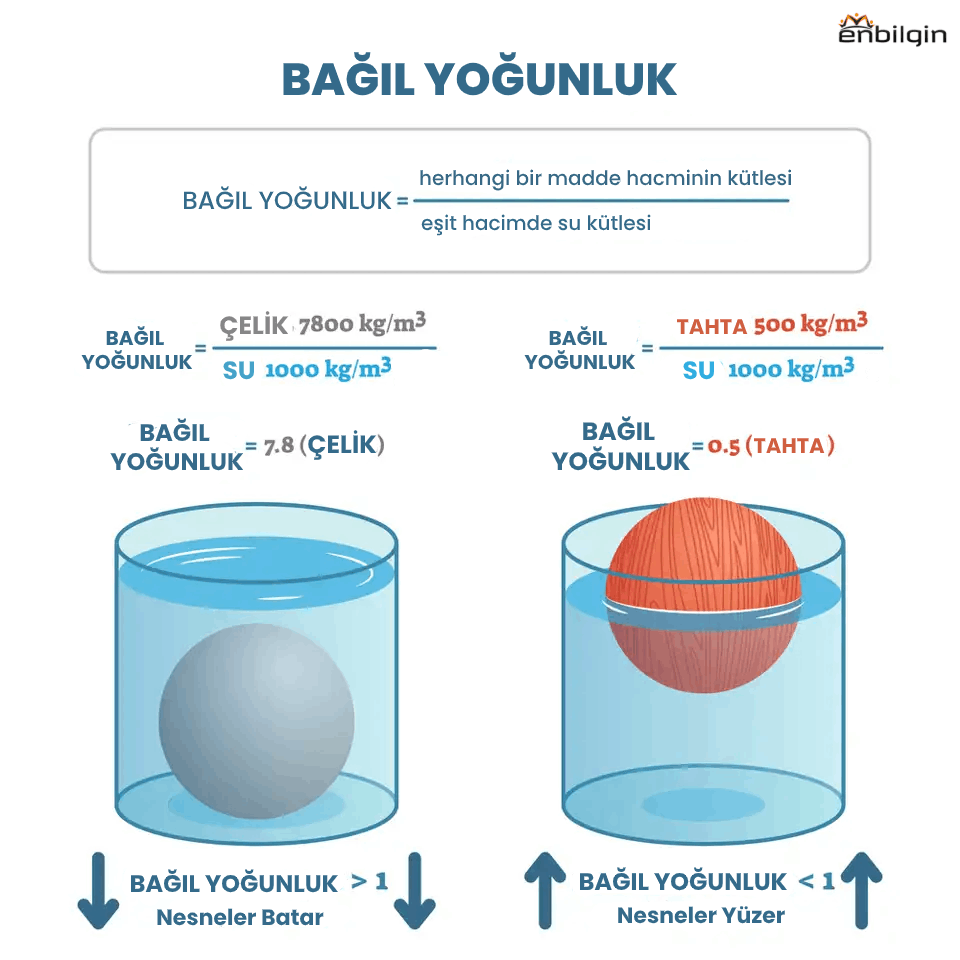 bağıl yoğunluk ile ilgili bir görsel. hacim olarak aynı boyuttaki çelik ve tahtadan oluşan nesneleri, 1000 kg/m³ suya bırakılmıştır. bu nesnelerin fiziksel özelliklerine bağlı olarak tahtanın yüzmesine ve çeliğin ise dibe batmasına neden olmuştur. bu resimde ağırlıktan bahsedilmemiştir. sadece hacim vardır. yani boyut
bağıl yoğunluk ile ilgili bir görsel. hacim olarak aynı boyuttaki çelik ve tahtadan oluşan nesneleri, 1000 kg/m³ suya bırakılmıştır. bu nesnelerin fiziksel özelliklerine bağlı olarak tahtanın yüzmesine ve çeliğin ise dibe batmasına neden olmuştur. bu resimde ağırlıktan bahsedilmemiştir. sadece hacim vardır. yani boyut
Fiziksel özellikler hacim ve kütledir. Değeri, ölçtüğümüz madde miktarına bağlıdır. Maddenin yoğun özellikleri Renk, Yoğunluk, Kaynama Noktası ve Erime Noktasıdır. Bunlar kalıcıdır; madde miktarına bağlı olarak değişmezler.
Burada bahsedebileceğimiz başka özellikler de var, ancak bunlar en önemli olarak kabul edilen bu altı maddenin altında yer almaktadır. Maddenin belirtilmesi gereken diğer özellikleri, örneğin kırılma indisi, sıcaklık ve sertliktir. Bunların tümü, genellikle toplu özellikler olarak tanımlanan yoğun özelliklerdir. Ölçtüğümüz sistemin boyutuna veya bu sistemde bulunabilecek malzeme miktarına bağlı değildirler.

Yanma ısısı, madde oksijen kullanımıyla tamamen yanınca ortaya çıkan enerjinin özelliğidir. Bu özellik, böyle bir reaksiyon sırasında açığa çıkan enerji miktarını ölçer. Kimyasal kararlılık, bir maddenin belirli bir ortama yerleştirildiğinde tepki verip vermeyeceğini belirleyen özelliktir. Çoğunlukla bir bileşiği suya yerleştirerek veya sadece hava ile nasıl reaksiyona girdiğini görmek için dışarıda bırakarak gözlemlenir. Bu reaksiyonlara hidroliz ve oksidasyon denir.
Bir sonraki kimyasal özellik yanma kabiliyetini ölçen yanıcılıktır. Yanıcılık sayesinde, maddenin ateşe maruz kaldıktan sonra yanıp yanmayacağını görebiliriz. Yanma kimyasal bir reaksiyondur ve altına madde koyarak, ne kadar yanıcı olduğunu ve ne kadar çabuk yanacağını belirleyebiliriz. Son olarak, tercih edilen oksidasyon durumu, belirli bir bileşiğin, en az miktarda enerji gerektiren oksidasyon seviyesini belirler. Oksidasyon durumu, genel olarak, bir bileşiğin oksidasyon derecesi (elektron kaybı) ve tercih edilen, en düşük miktarda enerjiye ihtiyaç duyanıdır.
Fiziksel Özellikler; Bir maddenin kimyasal bileşimini değiştirmeden ölçülebilen veya gözlemlenebilen özelliklerdir. Hacim ve renk gibi şeyler bu kategoriye girer.
Kimyasal Özellikler; Sadece bir maddenin kimyasal kimliğini değiştirdiğimizde ölçülebilir veya gözlemlenebilir.
Kapsamlı ve yoğun özellikler sadece fiziksel özelliklerdir, ancak iki özel gruba ayrılır. Hacim ve kütle gibi geniş özellikler, ölçtüğümüz madde miktarına bağlı olarak, renk ve yoğunluk gibi yoğun özellikler yoktur.
Fiziksel Özellikler
Altı ana fiziksel özellik vardır. Ölçebilmemiz veya gözlemleyebilmemiz için, maddenin bileşimini değiştirmeye gerek yoktur. Altı fiziksel özellik Renk, Yoğunluk, hacim, kütle, kaynama noktası ve erime noktasıdır. Bu altıdan dördü yoğunluk ile ilgili, diğer ikisi ise genişlik ile ilgilidir.
Fiziksel özellikler hacim ve kütledir. Değeri, ölçtüğümüz madde miktarına bağlıdır. Maddenin yoğun özellikleri Renk, Yoğunluk, Kaynama Noktası ve Erime Noktasıdır. Bunlar kalıcıdır; madde miktarına bağlı olarak değişmezler.
Burada bahsedebileceğimiz başka özellikler de var, ancak bunlar en önemli olarak kabul edilen bu altı maddenin altında yer almaktadır. Maddenin belirtilmesi gereken diğer özellikleri, örneğin kırılma indisi, sıcaklık ve sertliktir. Bunların tümü, genellikle toplu özellikler olarak tanımlanan yoğun özelliklerdir. Ölçtüğümüz sistemin boyutuna veya bu sistemde bulunabilecek malzeme miktarına bağlı değildirler.
Kimyasal Özellikler
Daha önce de belirttiğimiz gibi, kimyasal özellikler sadece ölçtüğümüz maddenin kimyasal yapısını değiştirerek ölçebileceğimiz özelliklerdir. Bu özelliklerin bir kimyasal reaksiyonun içine yerleştirildiğinde maddenin nasıl davrandığını ölçtüğü anlamına gelir. Bu özellikler sadece böyle bir reaksiyon sırasında ortaya çıkabilir. En önemli dört kimyasal özellik Yanma ısısı, Kimyasal kararlılık, Yanıcılık ve tercih edilen Oksidasyon durumudur.
Yanma ısısı, madde oksijen kullanımıyla tamamen yanınca ortaya çıkan enerjinin özelliğidir. Bu özellik, böyle bir reaksiyon sırasında açığa çıkan enerji miktarını ölçer. Kimyasal kararlılık, bir maddenin belirli bir ortama yerleştirildiğinde tepki verip vermeyeceğini belirleyen özelliktir. Çoğunlukla bir bileşiği suya yerleştirerek veya sadece hava ile nasıl reaksiyona girdiğini görmek için dışarıda bırakarak gözlemlenir. Bu reaksiyonlara hidroliz ve oksidasyon denir.
Bir sonraki kimyasal özellik yanma kabiliyetini ölçen yanıcılıktır. Yanıcılık sayesinde, maddenin ateşe maruz kaldıktan sonra yanıp yanmayacağını görebiliriz. Yanma kimyasal bir reaksiyondur ve altına madde koyarak, ne kadar yanıcı olduğunu ve ne kadar çabuk yanacağını belirleyebiliriz. Son olarak, tercih edilen oksidasyon durumu, belirli bir bileşiğin, en az miktarda enerji gerektiren oksidasyon seviyesini belirler. Oksidasyon durumu, genel olarak, bir bileşiğin oksidasyon derecesi (elektron kaybı) ve tercih edilen, en düşük miktarda enerjiye ihtiyaç duyanıdır.
 Türkiye'nin en güncel forumlardan olan forumdas.com.tr'de forumda aktif ve katkısı olabilecek kişilerden gönüllü katkıda sağlayabilecek kişiler aranmaktadır.
Türkiye'nin en güncel forumlardan olan forumdas.com.tr'de forumda aktif ve katkısı olabilecek kişilerden gönüllü katkıda sağlayabilecek kişiler aranmaktadır.